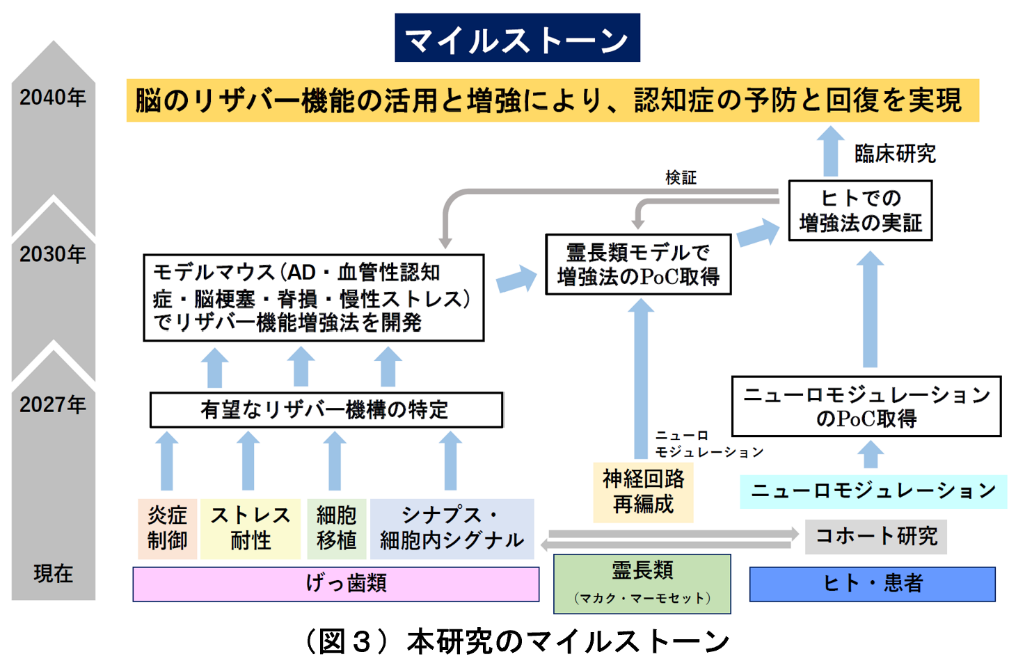
従来の認知症研究は、例えばアルツハイマー病(AD)に関しては、アミロイドβ(Aβ)とリン酸化タウの蓄積という病理(AD病理)が主原因とされ、それらの産生を阻害ないしは除去を目指す研究が主流だった。しかし、近年開発されたヒト化抗Aβ抗体レカネマブの投与によってAD病理が抑制されても、認知症の進行は遅らせることはできるが完全には止められないことが明らかになった。これは一旦AD病理が進行すると、そのままでは脳機能を回復しないことを意味する。従って機能を回復するためには全く異なったアプローチも必要である。そこで、本研究では「脳のレジリエンスを支えるリザバー機能」に着目する。ここでいうリザバー機能とは、神経細胞の可塑性に裏付けられる脳の余剰能力である。研究開発代表者はこれまで主として霊長類モデルを用いて脳・脊髄損傷後の機能回復機構を研究してきたが、その過程で様々なリザバー機能を見出し、その増強法の開発を試みてきた。そこで次に検証したい仮説として慢性的な神経変性疾患、ストレス障害と急性の中枢神経系損傷に対してある程度共通のリザバー機能が存在すると考えた。本研究課題では、今後の20年余りを展望しての認知症対策として、このような神経変性疾患や中枢損傷や慢性ストレスを克服するための脳のリザバー機能の実体を明らかにし、上記の仮説の検証を試みるとともに、その増強法の開発を目指す。リザバー機能には多様な階層と作用機序が存在し得る。特に1.急性・慢性の障害双方において障害を免れて残存する回路機能を促進する、2.障害されつつある細胞を回復させる、3.進行性の障害において障害の進行を止める(図1)。
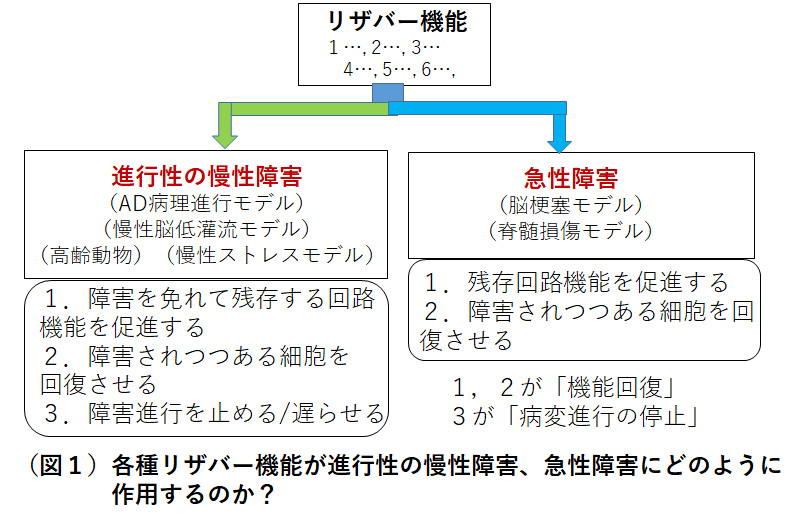
そこで本研究課題では、様々な脳のリザバー候補の脳内機構を専門とする研究チームを集め、連携して、図1のように各自が検討しているリザバー機能を促進する手法について、各種障害モデルを対象として取り組む。そこでは、主としてげっ歯類を用いるグループには、(1)シナプス可塑性や細胞内シグナル伝達チームとして、シナプス可塑性の閾値を調整する技術の開発と実証(林)、神経細胞の「健常さ」の指標となり機能回復に寄与するシグナル分子の同定(渡邉)、人工シナプスコネクターによる可塑性の増強(柚﨑、武内)が参画する。さらに、(2) 脳内の炎症・免疫とグリア細胞チームとして、疾患関連ミクログリアの特定と特徴づけ(大槻)、免疫炎症におけるミクログリアの多様性の喪失と治療戦略(和氣)、セロトニル化という翻訳後修飾機能に着目した脳腸軸を介する脳のリザバー機能の解明(Fagarasan)。(3)ストレス応答研究チームは、ストレス感受性・耐性の基盤となる慢性炎症の分子機序とその制御(古屋敷)、ストレスレジリエンスに関わる神経回路の同定と変容の分子機構(内田)を解明する。さらに、(4)高橋チームはiPS細胞由来脳オルガノイドの移植による増強法、(5)田口チームは造血幹細胞移植による海馬神経新生の活性化による増強法に取り組む。これらのグループでは、進行性の慢性障害を呈するAD病理進行モデルマウス(NL-G-Fマウス、5xFADマウスなど)、血管性認知症を想定した慢性脳低灌流モデル、高齢モデル、慢性ストレスモデルマウスと、一方で急性障害を示す脳梗塞や脊髄損傷モデルマウス等の複数のマウスモデルを用いて各分担研究者が対象とするリザバー機能の解明と促進法が作用するメカニズムの解明に取り組む。そして非ヒト科霊長類(マカクザル、マーモセット)を用いるグループ(山口、肥後、梅田)は、ニューロモジュレーション法等による成熟脳での大規模回路の可塑性誘導とその遺伝子基盤を解明し、げっ歯類で得られたリザバー機能増強法の有効性を老齢や脳低灌流マーモセットや急性の脳梗塞、脊髄損傷または脳低灌流モデルマカクザルなどの霊長類モデルで検証する。霊長類モデルにおいては専門家と連携して病理学的な検証を慎重に行う。そしてヒトを対象とする研究グループでは、ニューロモジュレーションとして、脳の複数部位を位相変調させて刺激するアンサンブル型脳刺激法を開発し、リザバー機能の増強を目指す(美馬、小金丸)。また、松本チームはコホート研究を基盤として、運動・認知の二重課題による認知レジリエンス増強効果の脳波による生理指標を開発する。そして花川チームは認知症患者を含む高齢者のMRIコホート並びにヒト死後脳のMRI撮像と光学・質量顕微鏡の組織・分子情報統合研究から、加齢に抵抗して認知機能の維持を可能にするヒト脳のレジリエンス/リザバー機能の実体を探索し、得られる情報を他のグループに提供する。
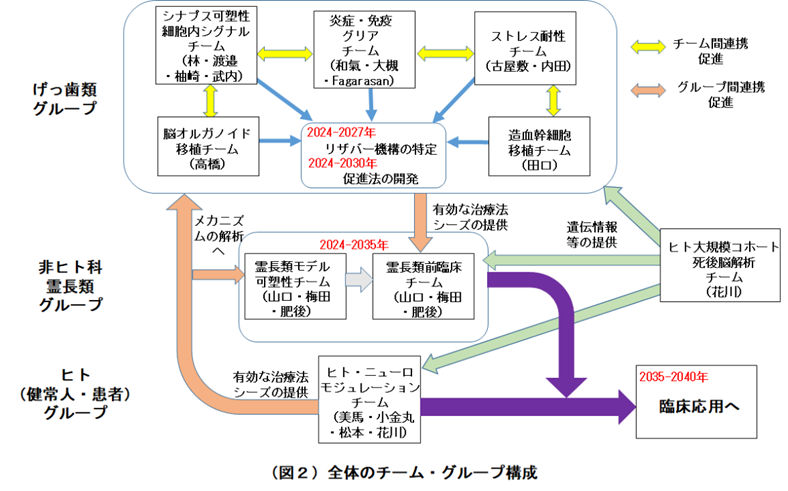
げっ歯類グループでは、2024-27年にそれぞれ有望なリザバー機能を特定し、2030年までに認知症モデルや脳梗塞・脊髄損傷モデルマウス等において増強法を開発する。特にADモデルマウスに対する増強法が、AD病理を進行させたまま機能改善するのか、AD病理の進行を止めるないしは消去するのかにも着目する。そして霊長類モデルでの検証、Proof of Concept (PoC)を取得する。他方、ヒト研究で有望な増強法についてげっ歯類、霊長類モデルでメカニズムを解明する。このようにして、げっ歯類やヒトでの成果を霊長類モデルでの検証を含むPoCの取得につなげるのが本研究の狙いである。それにより多くの課題について2035年までに前臨床として霊長類モデルでのPoCの取得、2040年でのヒト臨床試験につなげる。そのためには、各チームの研究が同じ現象の表と裏を見ている可能性もあるので各チーム間の連携・共同研究を重点的に推進する。