林 康紀

氏名Name
林 康紀
所属・職名Affiliation, Title, etc.
京都大学大学院医学研究科 システム神経薬理学分野 教授
研究室HPWebsite
一言メッセージShort Message
本プロジェクトでの研究概要Outline of the research in this project
損傷を受けた脳部位の機能を最大限に活かすためには、リザバーとなる神経細胞が適切に回路に組み込まれる必要がある。従来のシナプスタンパク質の過剰発現では、シナプスや回路の選択性がなく、脳の情報を適切に処理できないという問題があった。そこで、シナプス可塑性の閾値を下げつつ、その協同性、入力特異性、連合性といった特徴を保つ方法を開発する。そのため、シナプス可塑性を促進するためにカルモジュリンキナーゼ(CaMK)経路とCREBに着目する。これらの分子は、過剰発現によりシナプス可塑性の閾値を低下させ、可塑的変化を促進する。そこで、これらのシグナル経路を化学遺伝学や光遺伝学的手法に制御する方法を確立することで、シナプス可塑性を制御する。その後、老齢マウスやアルツハイマー病モデルマウスに適用して記憶能力の改善を検討する。最終的には、同様の手法がマーモセットにも適用可能かどうかを検討していく。
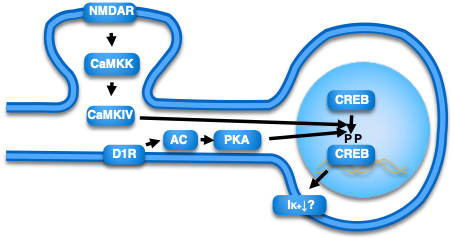
NMDA受容体からCaMKIV-CREB経路を介した神経興奮性の調節経路系路
これまで主な研究内容Outline of main research so far
我々は、一過性のシナプス入力増強が長期的なシナプス強化を引き起こす長期増強(LTP)を、記憶の細胞モデルとして研究してきた。そのために、遺伝子導入技術や二光子顕微鏡、FRETを駆使した解析を行ってきた。まず、LTP時にAMPA受容体がシナプスへ移行することを示し、CaMKIIの活性化が必要十分である一方で、受容体のリン酸化は不要であることを明らかにした。また、シナプス可塑性に関与するキナーゼであるCaMKIIが、活性化により液-液相分離を起こし、他のタンパク質の凝縮を誘導することを発見し、これがLTP時のシナプスへの分子移動と蓄積を制御する可能性を提唱した。さらに、LTPによりスパインが拡大し、アクチン重合が促進されることをFRETを用いて証明した。CaMKIIがF-アクチンと相互作用し、活性化によりその結合が解除されることで、LTP中のアクチン修飾が可能になることを見出した。
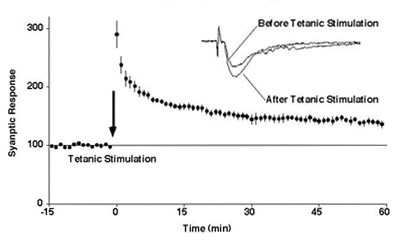
LTP in hippocampal CA1 region
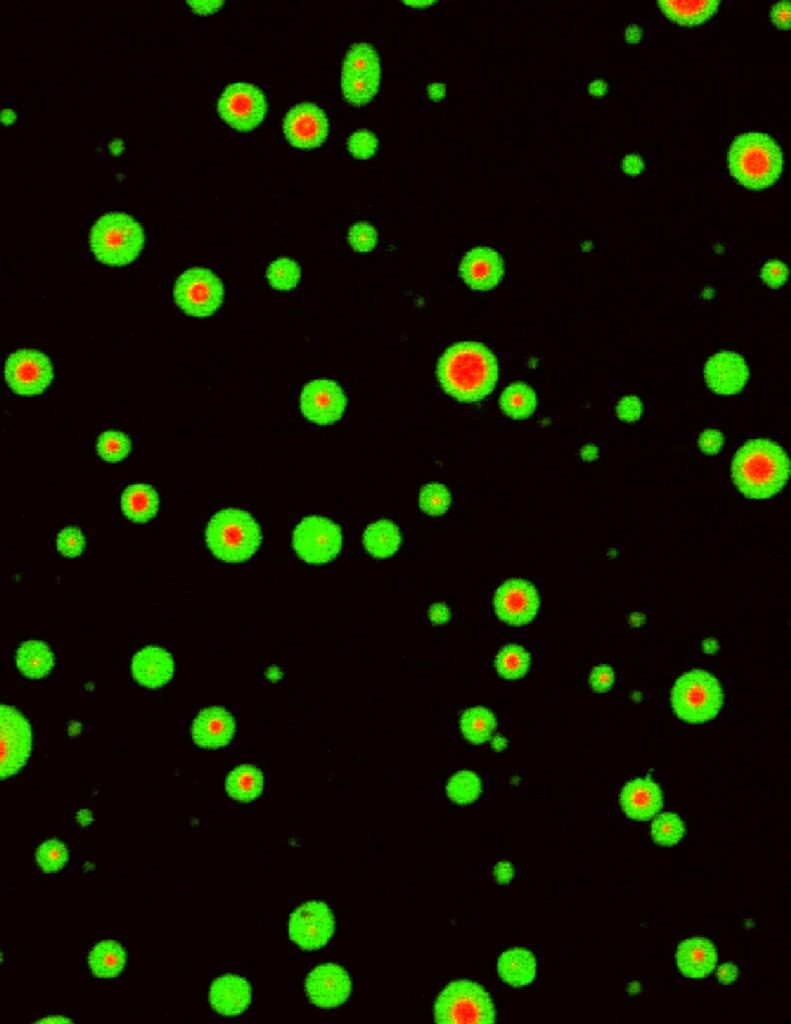
Liquid-liquid phase separation of CaMKII
Activation of CaMKII induces segregation of NMDA receptors (green) and AMPA receptor (red).
主な経歴・受賞歴等Career, Awards, etc.
Career
- 1984 - 1990
- Kyoto University Faculty of Medicine, MD
- 1990 - 1994
- Institute for Immunology and Department of Pharmacology, Kyoto University Faculty of Medicine, PhD
- 1994 - 1996
- Postdoctral Fellow, Department of Neurophysiology Institute for Brain Research, Faculty of Medicine, University of Tokyo
- 1996 - 2000
- Postdoctral Fellow, Cold Spring Harbor Laboratory
- 2000 - 2009
- Assistant Professor (joint), RIKEN-MIT Neuroscience Research Center, Massachusetts Institute of Technology
- 2009 - 2013
- Team Leader, Brain Science Institute, RIKEN
- 2013 - 2017
- Senior Team Leader, Brain Science Institute, RIKEN
- 2016 -
- Professor Kyoto University Graduate School of Medicine, Department of Pharmacology
Awards
- 2008
- JSPS Prize for Young Investigators
- 2008
- Japan Academy Medal
- 2019
- Toshihiko Tokizane Memorial Award
- 2021
- Setsuro Ebashi Award
主要業績Major Publications
Ripoli, C., Dagliyan, O., Renna, P., Pastore, F., Paciello, F., Sollazzo, R., Rinaudo, M., Battistoni, M., Martini, S., Tramutola, A., Sattin, A., Barone, E., Saneyoshi, T., Fellin, T., Hayashi, Y., and Grassi, C. (2023). Engineering memory with an extrinsically disordered kinase. Sci Adv 9, eadh1110.
https://doi.org/10.1126/sciadv.adh1110
Yasuda, R., Hayashi, Y., and Hell, J.W. (2022). CaMKII: a central molecular organizer of synaptic plasticity, learning and memory. Nat Rev Neurosci.
https://doi.org/10.1038/s41583-022-00624-2
Özden, C., Sloutsky, R., Mitsugi, T., Santos, N., Agnello, E., Gaubitz, C., Foster, J., Lapinskas, E., Esposito, E.A., Saneyoshi, T., Kelch, B.A., Garman, S.C., Hayashi, Y., and Stratton, M.M. (2022). CaMKII binds both substrates and activators at the active site. Cell reports 40, 111064.
https://doi.org/10.1016/j.celrep.2022.111064
Hosokawa, T., Liu, P.W., Cai, Q., Ferreira, J.S., Levet, F., Butler, C., Sibarita, J.B., Choquet, D., Groc, L., Hosy, E., Zhang, M., and Hayashi, Y. (2021). CaMKII activation persistently segregates postsynaptic proteins via liquid phase separation. Nat Neurosci 24, 777-785.
https://doi.org/10.1038/s41593-021-00843-3
Goto, A., Bota, A., Miya, K., Wang, J., Tsukamoto, S., Jiang, X., Hirai, D., Murayama, M., Matsuda, T., McHugh, T.J., Nagai, T., and Hayashi, Y. (2021). Stepwise synaptic plasticity events drive the early phase of memory consolidation. Science 374, 857-863.
https://doi.org/10.1126/science.abj9195
Sato, M., Mizuta, K., Islam, T., Kawano, M., Sekine, Y., Takekawa, T., Gomez-Dominguez, D., Schmidt, A., Wolf, F., Kim, K., Yamakawa, H., Ohkura, M., Lee, M.G., Fukai, T., Nakai, J., and Hayashi, Y. (2020). Distinct Mechanisms of Over-Representation of Landmarks and Rewards in the Hippocampus. Cell reports 32, 107864.
https://doi.org/10.1016/j.celrep.2020.107864
Saneyoshi, T., Matsuno, H., Suzuki, A., Murakoshi, H., Hedrick, N.G., Agnello, E., O'Connell, R., Stratton, M.M., Yasuda, R., and Hayashi, Y. (2019). Reciprocal Activation within a Kinase-Effector Complex Underlying Persistence of Structural LTP. Neuron 102, 1199-1210 e1196.
https://doi.org/10.1016/j.neuron.2019.04.012
Kim, K., Lakhanpal, G., Lu, H.E., Khan, M., Suzuki, A., Kato-Hayashi, M., Narayanan, R., Luyben, T.T., Matsuda, T., Nagai, T., Blanpied, T.A., Hayashi, Y., and Okamoto, K. (2015). A temporary gating of actin remodeling during synaptic plasticity consists of the interplay between the kinase and structural functions of CaMKII. Neuron 87, 813-826.
https://doi.org/10.1016/j.neuron.2015.07.023
Hosokawa, T., Mitsushima, D., Kaneko, R., and Hayashi, Y. (2015). Stoichiometry and phosphoisotypes of hippocampal AMPA type glutamate receptor phosphorylation. Neuron 85, 60-67.
https://doi.org/10.1016/j.neuron.2014.11.026
Bosch, M., Castro, J., Saneyoshi, T., Matsuno, H., Sur, M., and Hayashi, Y. (2014). Structural and molecular remodeling of dendritic spine substructures during long-term potentiation. Neuron 82, 444-459.
https://doi.org/10.1016/j.neuron.2014.03.021



